Ученые из Международного научно-исследовательского института животноводства (ILRI), Ливерпульского университета, Эдинбургского университета и других стран проследили, как системы животноводства действуют как резервуар для бактерий, устойчивых к противомикробным препаратам (УПП), и генетических детерминант УПП, которые могут инфицировать или колонизировать людей.
Это проливает свет на факторы, влияющие на УПП на пересечении нескольких видов и сектора «Единое здравоохранение». Исследование, проведенное в Найроби, Кения, опубликовано в выпуске BMC Medicine на этой неделе и помогает подробно описать, как избежать и управлять развитием лекарственной устойчивости у бактерий.
Александр Флеминг, открывший первый в мире антибиотик пенициллин, предупредил, что неправильное использование антибиотиков может привести к УПП. Он показал, что бактерии, вирусы, грибки и паразиты развиваются при воздействии антибиотиков и в конечном итоге перестают реагировать на эти лекарства. В результате лекарственной устойчивости антибиотики и другие противомикробные препараты становятся неэффективными, а лечение инфекций становится все более трудным или невозможным.
Сегодня УПП встречается во всем мире и представляет собой серьезную проблему. Подсчитано, что если проблему не решить сейчас, то к 2050 году каждые три секунды из-за УПП будет умирать один человек.
«Страны с высоким уровнем дохода могут использовать ресурсы и крупные инвестиции для борьбы с УПП способами, которые не могут использовать страны с низким уровнем дохода », — пояснил ведущий научный сотрудник Дишон Мулои, научный сотрудник Международного научно-исследовательского института животноводства (ILRI) и бывший доктор философии. студент Эдинбургского университета.
«Но УПП — это не просто проблема с высоким уровнем дохода или проблема страны с низким уровнем дохода. Учитывая легкость, с которой он может распространяться по всему миру, это общая проблема. клинике в Гонконге через два или три дня. Мы пока не решаем проблему с той срочностью, в которой она нуждается, учитывая наш взаимосвязанный мир».
Предполагается, что одним из путей развития УПП является большое количество антибиотиков, используемых в животноводстве, когда бактерии вырабатывают устойчивость и затем распространяются среди людей. Количественной информации по этому вопросу до сих пор было недостаточно. В сегодняшнем исследовании использовались геномика, эпидемиология и экология, чтобы изучить закономерности носительства гена AMR в образцовом организме E. coli.
В рамках контролируемой эпидемиологической оценки 99 домохозяйств в Найроби, Кения, ученые секвенировали полные геномы бактерий, выделенных из образцов экскрементов 311 человек, 606 крупного рогатого скота и 399 диких животных. Используя статистические модели, они изучили распространенность носительства УПП и описали разнообразие и структуру генов УПП в различных популяциях носителей по всему городу. Они также исследовали условия, которые могли привести к распространению генов AMR от людей к симпатрическим животным на уровне домохозяйств.
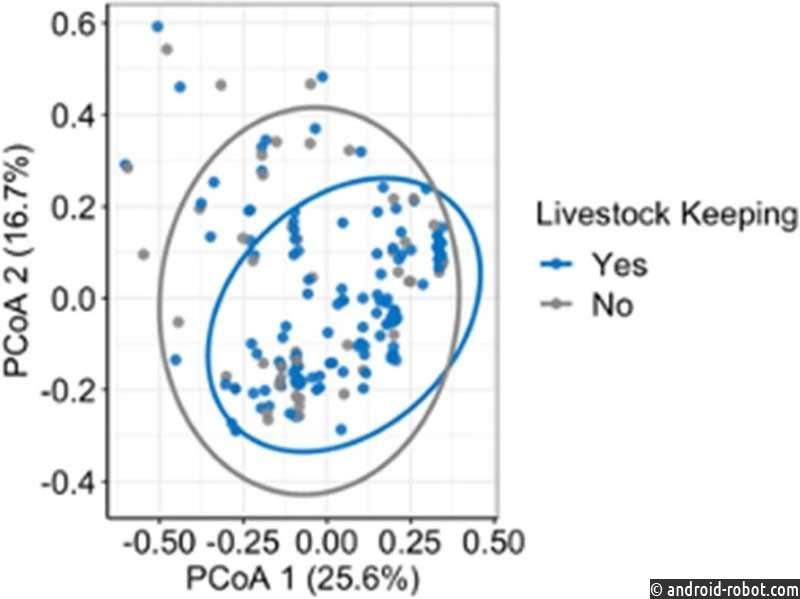
В изолятах животных и человека команда обнаружила 13 точечных мутаций и 56 приобретенных генов, которые, как известно, придают устойчивость к девяти различным классам антибиотиков. Они обнаружили, что состав сообщества генов AMR не связан с видом-хозяином, но что гены AMR часто располагались совместно, возможно, на плазмидах, что позволяет предположить, что множественная лекарственная устойчивость может быть приобретена и распространена за один шаг. Риск передачи УПП через контакты человека и домашнего скота наиболее высок при неправильной утилизации навоза и в больших домохозяйствах.
Из исследования вытекают два следствия для политики . Во-первых, необходимо подчеркнуть важность эпиднадзора за УПП в масштабах всей экосистемы. «Врачи должны думать не только о росте УПП у людей, но и у домашнего скота и в окружающей среде в целом, потому что мы видим, что дикие животные собирают и перемещаются с тем, что они получают из окружающей среды», — сказал Мулои.
Выводы исследования о широко распространенном носительстве клинически значимых механизмов УПП в популяциях людей и животных, особенно у диких животных, перемещающихся на большие расстояния, подчеркивают важность научно обоснованного эпиднадзора для борьбы с устойчивостью к противомикробным препаратам в глобальном масштабе.
«Это исследование показывает, как легко гены устойчивости к противомикробным препаратам перемещаются между людьми и домашним скотом в многолюдной городской среде, подчеркивая, что если мы хотим победить проблему устойчивости, нам потребуется скоординированный ответ в медицинском и ветеринарном секторах», — говорит Марк Вулхаус, профессор и Кафедра эпидемиологии инфекционных заболеваний Эдинбургского университета.
Во-вторых, проблема удаления навоза, которая может показаться обыденной, но очень важной. «Если вы проедете по Найроби, то увидите на дорогах кучи навоза», — сказал Мулои. «Традиционно мы не считали навоз проблемой, и даже если мы посмотрим на нашу политику, аналогичную политике многих других стран, навоз не рассматривается как риск. Но ясно, что нам нужно работать намного лучше. очистки окружающей среды во имя хорошего здоровья населения».
Исследование является частью общего проекта под названием «Городской зоопарк», или более формально известного как «Эпидемиология, экология и социально-экономические аспекты возникновения болезней в Найроби». По словам руководителя исследования Эрика Февра, профессора ветеринарных инфекционных заболеваний Института инфекционных, ветеринарных и экологических наук Ливерпульского университета и совместно назначенного главного научного сотрудника ILRI, цель состоит в том, чтобы понять механизмы, ведущие к интродукции и распространению патогенов в городских условиях. населения. «Здесь мы видим, что нам нужен целостный подход , который включает людей, животных, их отходы и общую среду», — говорит Февр.